Ionebytte – grunnleggende prinsipper
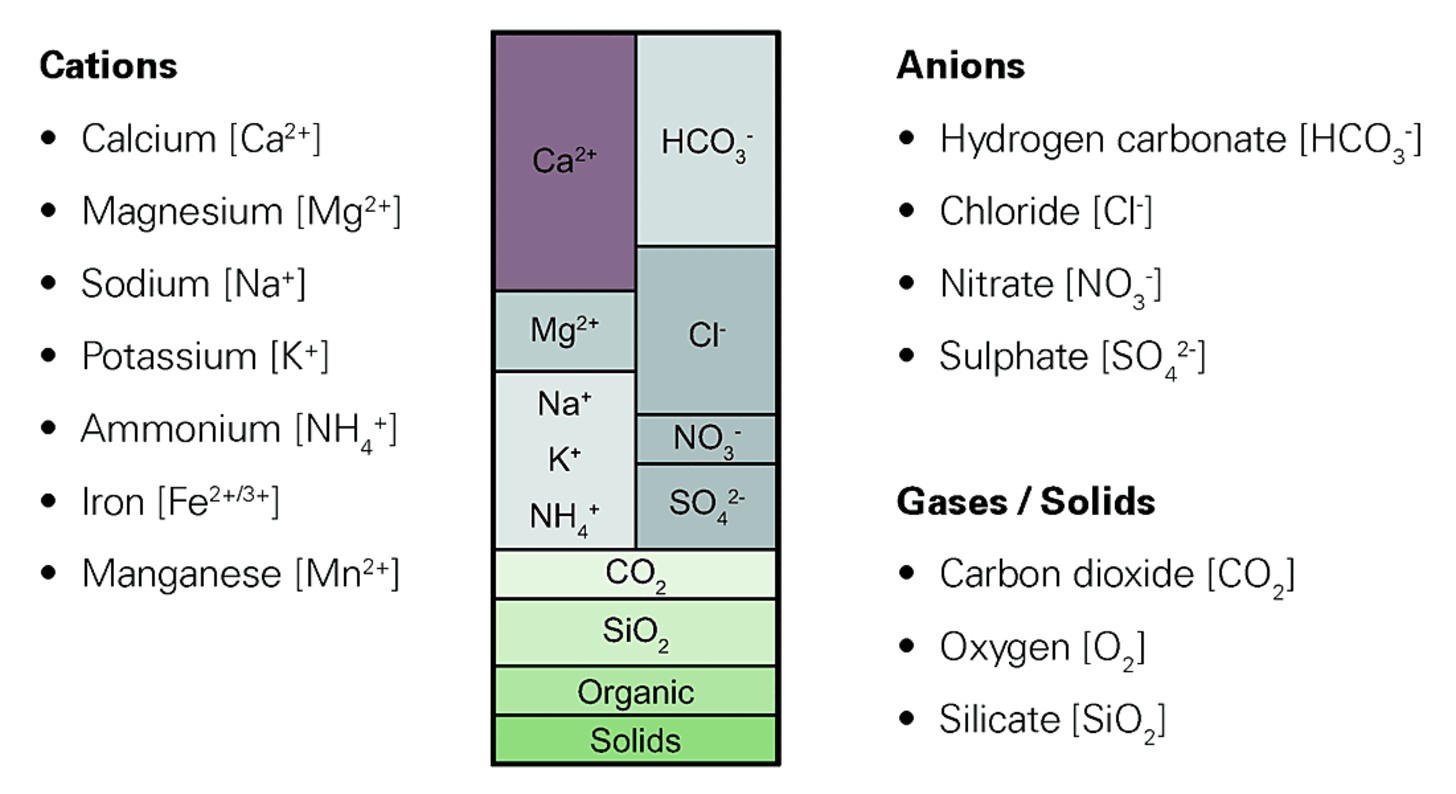
Vann er forbindelsen mellom hydrogen og oksygen som oppstår ved forbrenning av hydrogen. Det er et fremragende løsningsmiddel. Naturlig vann forekommer vanligvis ikke som kjemisk ren substans, men inneholder oppløste materialer og salter samt organiske forbindelser, men også disperse og kolloiddisperse stoffer som gasser – i forskjellige konsentrasjoner og sammensetninger.
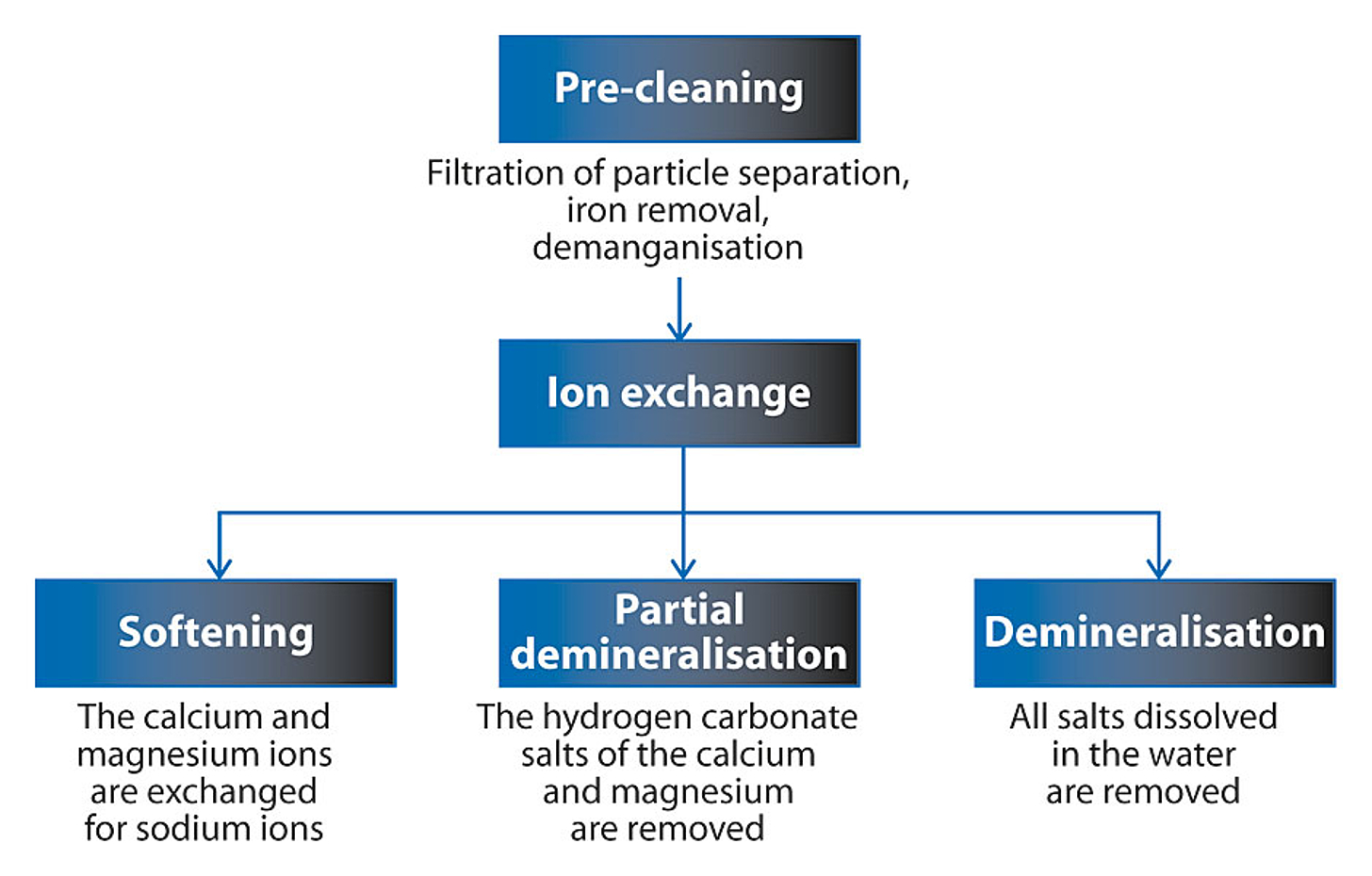
De oppløste saltene foreligger som ioner og kan fjernes fra vannet ved bruk av spesielle metoder.
Ionebytte – prinsipp
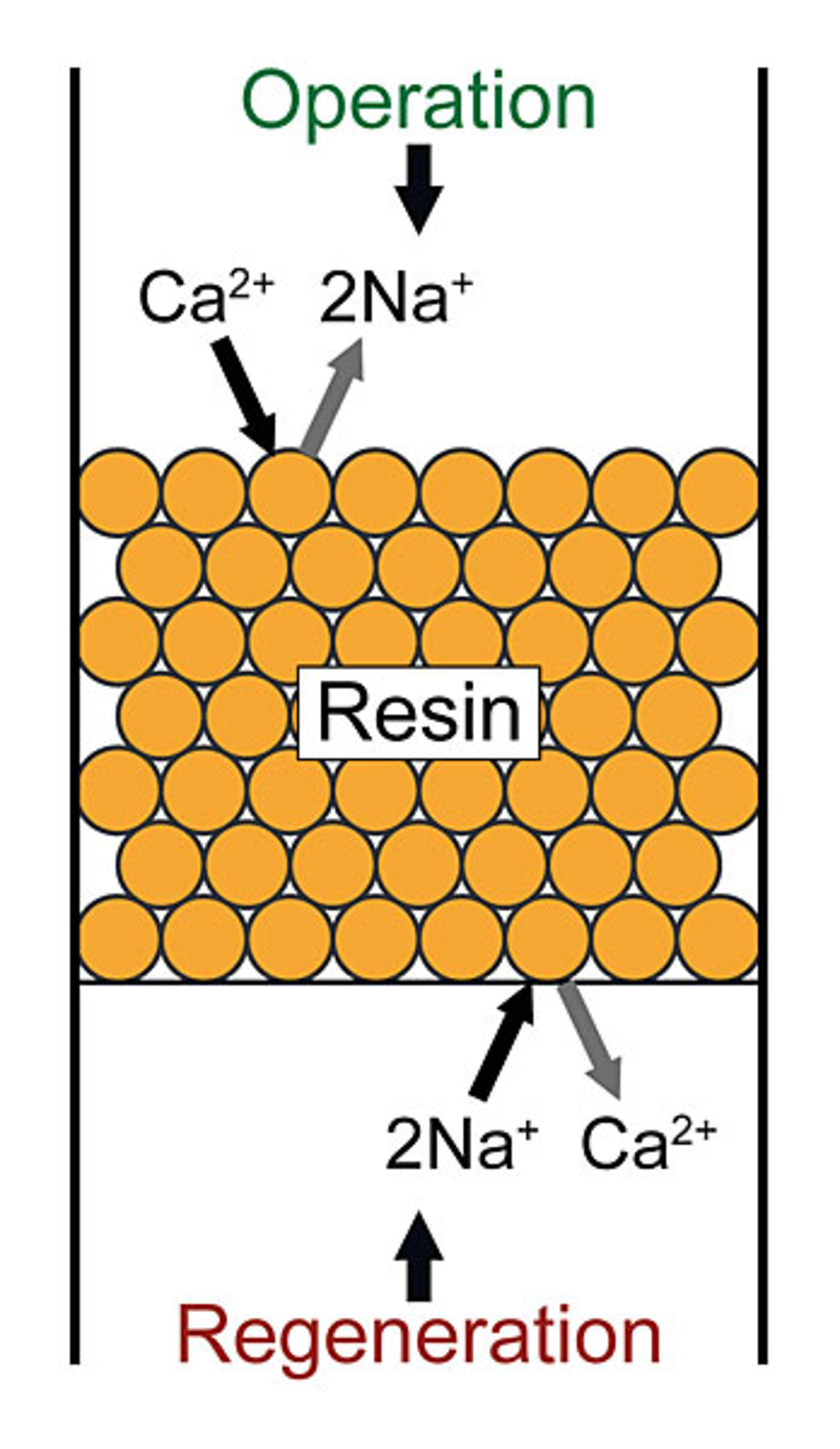
Ionebyttere er kunstharpiks (organiske polymere) med forskjellige innebygde bytteaktive grupper, som ioner avleires på. Ved byttingen blir ionene i løsningen som skal behandles, byttes ut med avleirede ioner med lik elektrisk ladning på harpiksen.
Man skiller prinsipielt mellom kationebyttere og anionebyttere. Innenfor disse typene er det ytterligere differensiering med hensyn til de bytteaktive gruppene:
- svakt sur / sterkt sur
- svakt basisk / middels basisk / sterkt basisk
Begrepene "ionebyttere" og "harpiks" brukes synonymt innen vannbehandling.
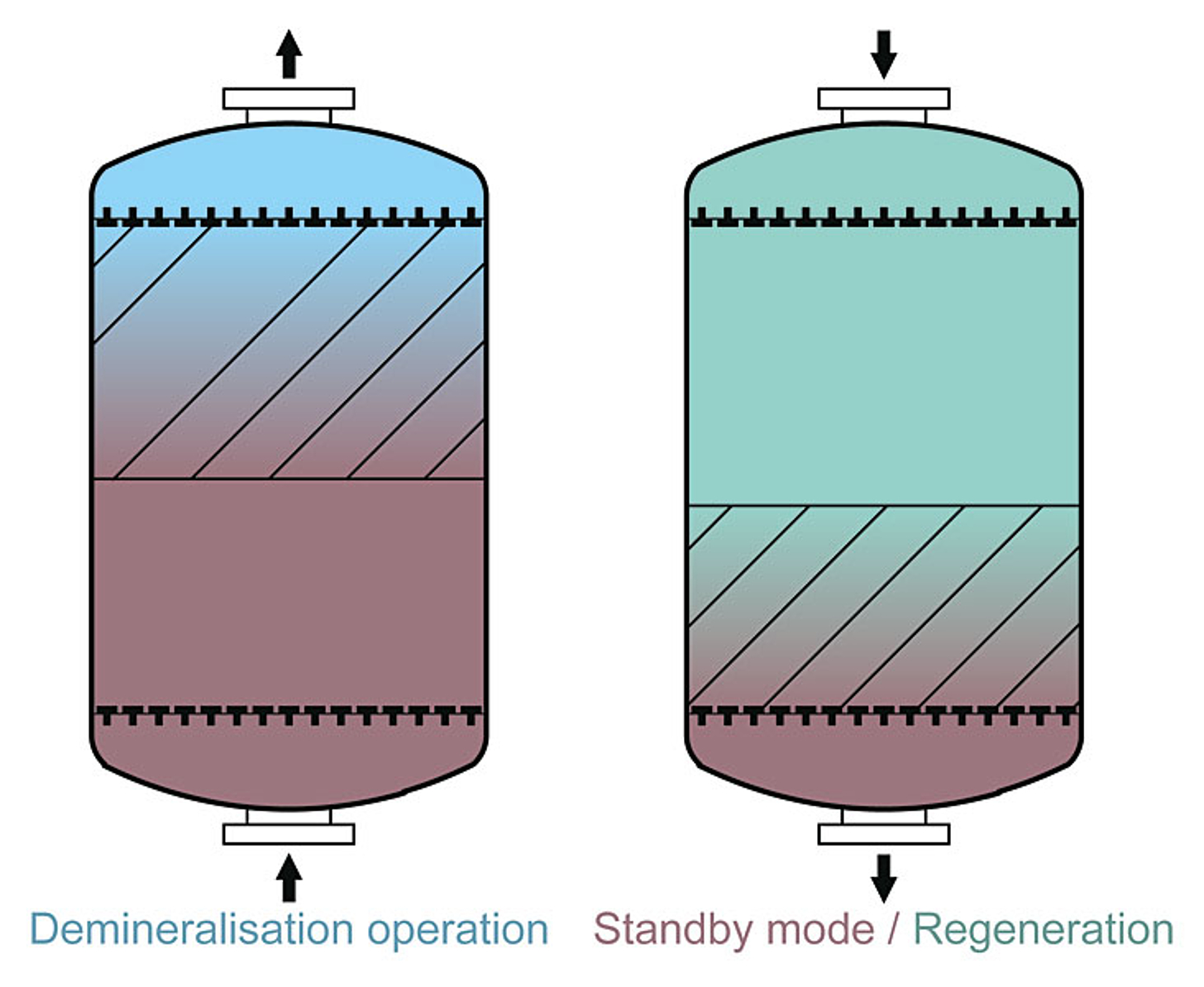
Fluidisert bad
På grunn av de mange fordelene brukes som oftest fluidisert bad i ionebytteanlegg.
Fordeler:
- svært effektiv utnyttelse av regenereringsmiddel kombinert med maksimal avsaltingseffekt
- store variasjonsmuligheter ved valg av harpiks
- lavt eget vannforbruk
- svært kompakt beholderkonstruksjon
Denne metoden forutsetter god forhåndsrensing av råvannet. Vannet må være fritt for jern, mangan og svevestoffer.